유전자 요법은 단일 투여를 통해 치료용 단백질의 발현을 지시하거나 누락된 단백질의 발현을 복원함으로써 유전 또는 후천적 질병이 있는 환자에게 장기적이고 잠재적인 치유적 이점을 제공합니다.
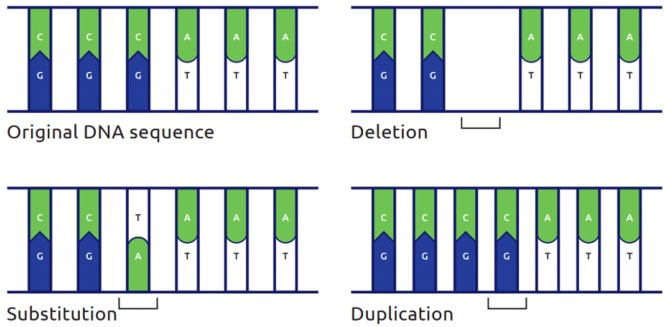
유전자는 신체의 세포 조직이 단백질을 만드는 데 사용하는 청사진을 제공하는 DNA의 특정 영역입니다. 특정 유전자의 결함 또는 돌연변이는 단백질을 발현할 수 없거나 능력을 감소시키거나 단백질의 기능성을 감소시킬 수 있습니다. 예를 들어, B형 혈우병 환자에서 혈액 응고에 필요한 단백질 생산과 관련된 유전자가 없거나 돌연변이된 경우, 이 환자의 혈액은 경미한 외상이나 수술 후에도 출혈을 멈출 만큼 충분히 응고되지 않습니다. 적절한 유전자 사본을 세포에 도입하면 출혈을 예방하는 혈액 응고 인자의 존재와 자연적 기능을 회복할 수 있습니다.
간단히 말해서 유전자 치료는 유전병을 치료하거나 예방하기 위한 조사적 접근법입니다. 유전자 치료 연구는 새로운 것이 아닙니다. 실제로 과학자들은 50년 이상 이를 조사하고 발전시켜 왔으며 많은 질병을 치료할 수 있는 방법을 찾을 수 있는 잠재력을 가지고 있습니다.
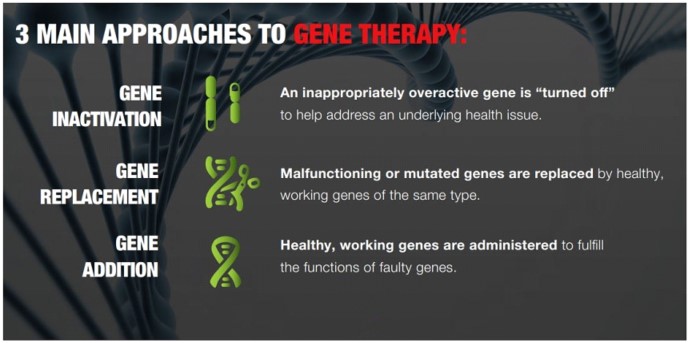
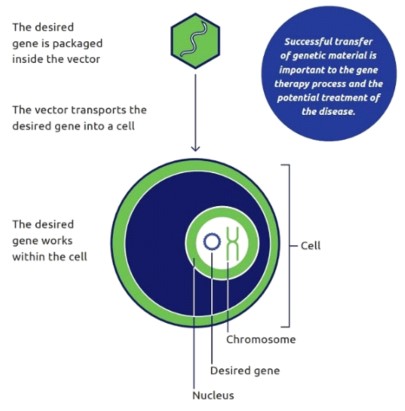
유전자 치료 연구의 목표는 질병을 치료하거나 신체가 질병과 싸우도록 돕기 위해 돌연변이 유전자를 대체하거나 비활성화하는 데 새로운 유전자를 사용할 수 있는지 여부를 결정하는 것입니다. 유전자가 세포 내로 전달되기 위해서는 일반적으로 트랜스포터(transporter)가 사용된다. 운반자는 벡터라고 합니다.