사람들의 삶을 변화시키기
환자, 그 가족, 의료 제공자, 질병 옹호 단체의 의견을 경청한 결과 우리의 임상 파이프라인 개발이 직접적으로 이루어졌습니다.
심부전 치료를 위해 삼중 이펙터 접근법을 활용하는 새로운 유전자 치료제 후보의 가능성을 평가하는 것은 세계 최초입니다.
환자, 그 가족, 의료 제공자, 질병 옹호 단체의 의견을 경청한 결과 우리의 임상 파이프라인 개발이 직접적으로 이루어졌습니다.
현재의 치료법은 삶의 질을 향상시키고 효율적인 비용과 잠재적인 부작용 감소로 장기적인 생존 이점을 보장할 수 있습니다.
심혈관 유전자 치료 설계 매트릭스(안전성과 효능의 균형)
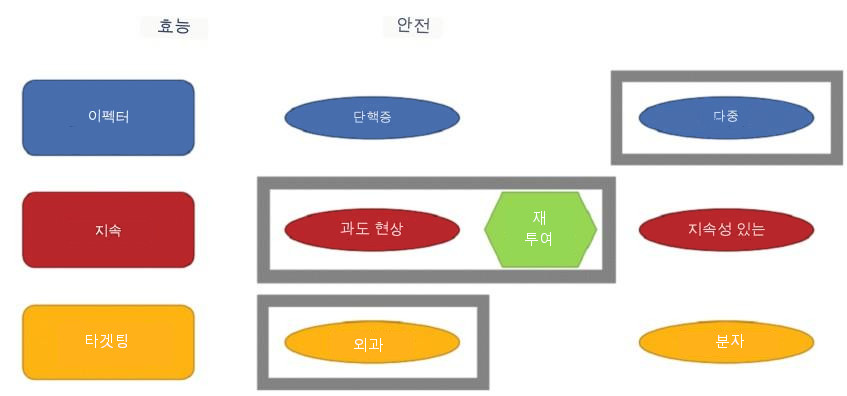
다유전자 벡터의 비바이러스 투여는 병리학적 심장 리모델링의 기본 분자 경로에 초점을 맞춥니다.
제넥스-3:: 삼중 이펙터 플라스미드
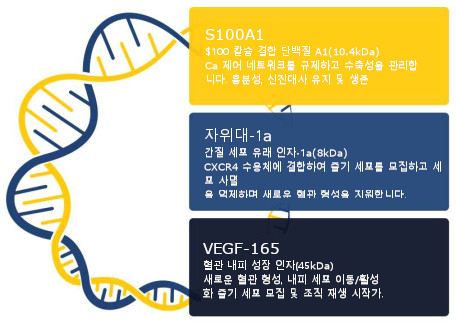
인간 질병 심근 세포에서 입증된 다유전자 접근법의 유용성
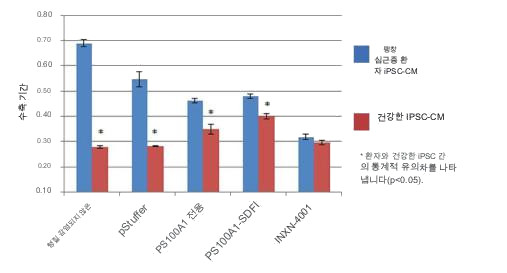
GENEX-3 형질감염은 환자 심근세포의 수축 기간을 개선합니다. 시험관 내
대조 세포와 비교하여 DCM iPSC-CM은 GENEX-3 형질감염 후 박동률, 수축 지속 시간 및 수축률에서 상당한 개선을 보였지만 세포 사멸의 증가는 보이지 않았습니다.
GENEX-3의 유리한 생체 분포 및 기능
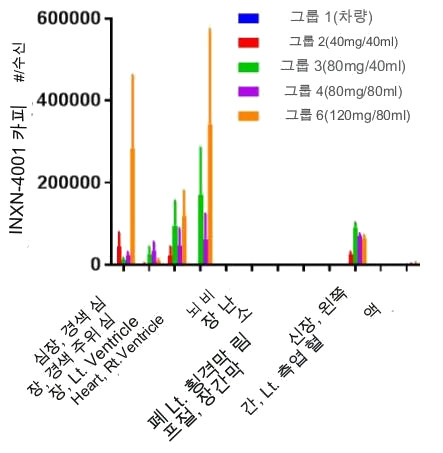
GENEX-3의 생체분포는 심장 특이적 전달을 나타냅니다.
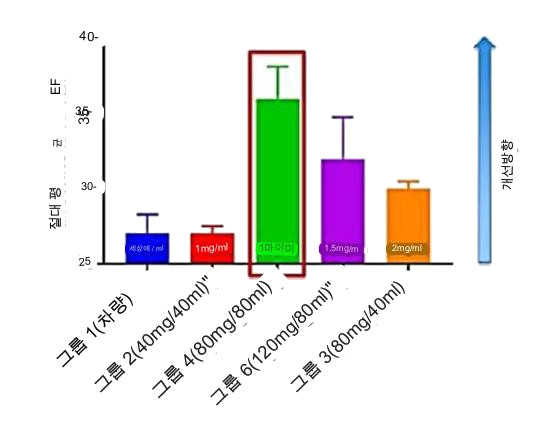
GENEX-3 용량에 대한 심근 기능 매개변수 비교는 EF의 증가를 나타냅니다.
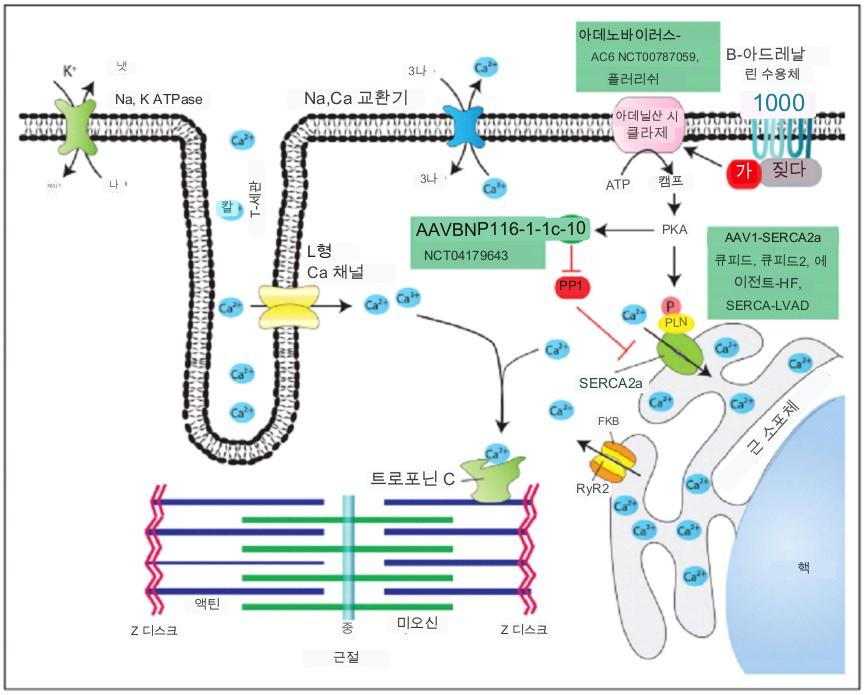
심근 세포 Ca2+ 주기를 통한 심장 흥분-수축 결합을 목표로 하는 우리의 현재 유전자 치료 전략이 상단 그림에 표시되어 있습니다.
RyR2 리아노딘 수용체는 심근 세포 원형질막이 탈분극될 때 근형질 세망 저장소에서 Ca2+ 방출을 제어하여 막의 L형 전압 의존성 Ca2+ 채널을 열어 미량의 Ca2+가 세포질로 들어가도록 합니다. troponin C에 결합하는 Ca2+는 많은 양의 Ca2+가 세포질로 유입되어 액틴과 미오신 사이의 생화학적 결합을 일으켜 수축을 일으킨다. FKBP12.6 단백질은 이완 기간 동안 RyR2가 기능하는 것을 방지합니다.
방출된 Ca2+는 부분적으로 ATPase SERCA2a에 의해 근형질 세망으로 재이송되고 부분적으로는 Na+/Ca2+ 교환기(NCX)에 의해 세포 외부에서 제거됩니다. SERCA2a 펌프 활동은 PLN(phospholamban)과의 연관성에 의해 규제됩니다. 인산화되지 않은 형태에서 PLB는 SERCA2a 활성을 방해합니다. 그러나 PLB의 인산화는 이러한 어려움을 방해합니다. 심근세포에서 PLB를 인산화(펌프 활성화 촉진)하는 주요 키나아제는 β-아드레날린성 자극에 의해 조절되는 PKA(단백질 키나아제 A)입니다. 특히, β-아드레날린성 수용체와 그 리간드의 결합은 헤테로삼량체 G 단백질을 활성화하여 수용체 복합체의 세포질 측에 위치한 AC(adenylate cyclase)를 활성화하여 ATP에서 cAMP로의 전환을 촉매합니다.
인산화 과정을 통한 PKA의 활성화는 심장 주기 내에서 세 가지 주요 구성 요소의 조절로 이어집니다. (2) 억제 단백질 FKB12.6의 해리를 촉진하는 RyR2; 및 (3) PLB, SERCA2a에 대한 억제 효과 감소. 결과적으로 이러한 변화는 주기 동안 칼슘 방출 및 재흡수의 효율성을 증폭시킵니다. 한편, PLN의 탈인산화는 주로 I-1c(억제제-1c)에 의해 억제되는 단백질 포스파타제-1(PP1)에 의존하는 SERCA2a의 비활성화를 유도합니다. 그림은 사용된 벡터와 임상 연구의 이름을 나타내는 SERCA2a, AC6 또는 I-1c(직사각형 녹색 상자)를 코딩하는 cDNA를 전송하여 심부전에서 이러한 경로 내에서 개입하는 세 가지 주요 의학적 접근법을 보여줍니다.
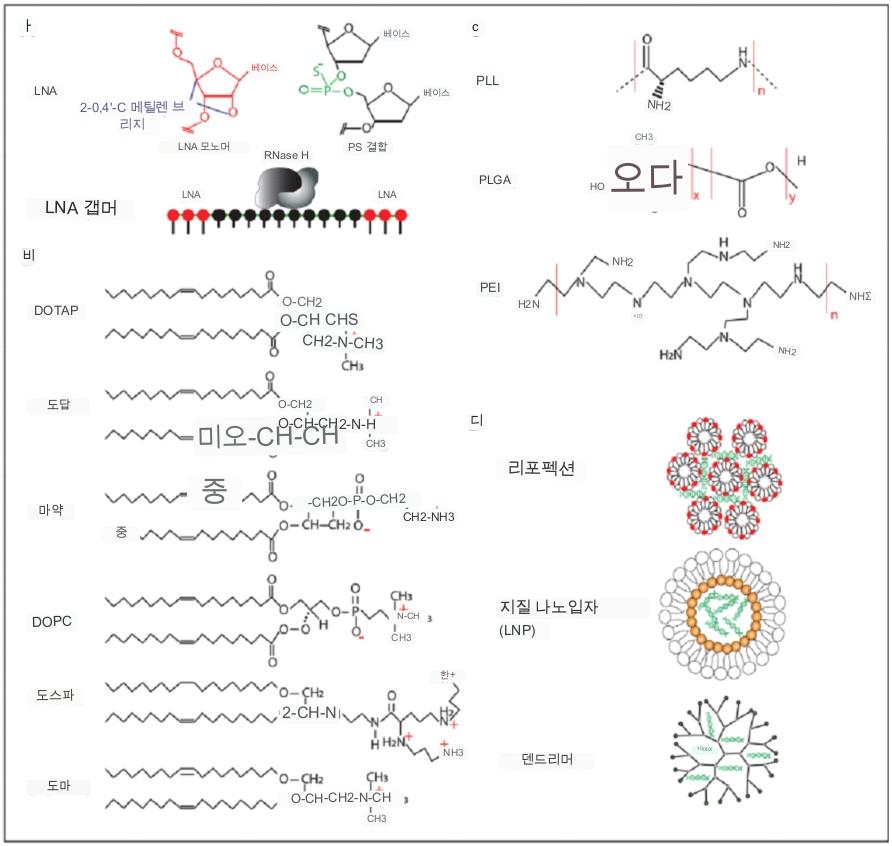
RNA 치료제 전달을 위한 분자 및 방법
패널의 왼쪽 상단에는 LNA 뉴클레오티드와 포스포로티오에이트 결합의 화학 구조가 표시되어 있습니다. 패널의 아래 부분은 LNA 갭머의 배열을 보여주며, 여기서 LNA 변형된 뉴클레오티드는 올리고뉴클레오티드의 두 말단에 배치되어 RNase H가 표적 RNA와 듀플렉스가 생성된 후 중간 부분에 도달할 수 있도록 합니다. 피>
리포펙션 및 지질 나노입자 형성에 사용되는 주요 양이온 및 중성 지질은 화학 구조로 식별할 수 있습니다. Polyplexes는 poly(ethylenimine) [PEI], polyL-lysine [PLL] 및 poly (lactic-co-glycolic acid) [PLGA]를 비롯한 다양한 주요 고분자 재료로 형성됩니다. 마지막 부분은 DNA와 나노 입자 구성 요소의 배열을 보여주는 개략도를 보여줍니다.
가장 최근 연구에서 SERCA2a cDNA의 방출과 같이 심근세포 형질도입에 크게 의존하는 대신 분비 단백질을 생산하는 애플리케이션이 더 효과적입니다. 이식을 받았거나 기계적 지지 장치 이식을 받은 치료받은 환자의 심장 샘플에서 AAV1.SERCA2a DNA의 양은 총 DNA50 마이크로그램당 43카피로 결정되었습니다(비교를 위해 1106개의 단핵 이배체 세포의 DNA 무게는 6g). SERCA2a가 세포 내에서 기능한다는 점을 감안할 때 이것은 의심할 여지 없이 긍정적인 결과였습니다. 손상되지 않은 내피(세포주위 투과성)로부터의 유출이 AAV 비리온과 같은 직경 20nm 크기의 입자에 대해 더 효과적이라는 사실에도 불구하고, CUPID 시험과 같은 벡터 관내 주입은 덜 침습적인 접근법입니다.
AAV1-SERCA2a는 초기 CUPID 연구(각각 25% 대 90%)와 비교하여 CUPID2 시험에서 더 많은 양의 빈 바이러스 벡터가 보고된 것이 또 다른 전달 관련 효능 요인이었습니다.
GENEX-3 임상 1상 연구 설계 및 현황
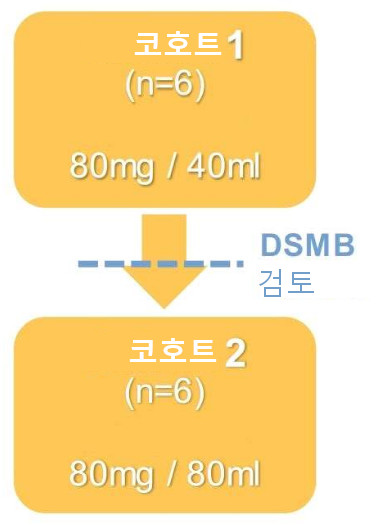
RCSI가 외래 환자 LVAD 환자를 대상으로 실시한 최초의 제1상 공개 라벨 안전성 연구에서 GENEX-3 투여
동일 용량의 GENEX-3(80mg)을 두 가지 용량(40mL 및 80mL)으로 20mL/분의 속도로 투여하는 안전성을 평가하기 위해 말기 HF의 기계적 지원은 각각 6명의 개인으로 구성된 두 개의 코호트로 나뉘었습니다.
RCSI 데이터는 다음 시점에 클리닉 방문 중에 수집되었습니다: 치료 전, 3일, 투약 후 1, 3, 6, 12개월.
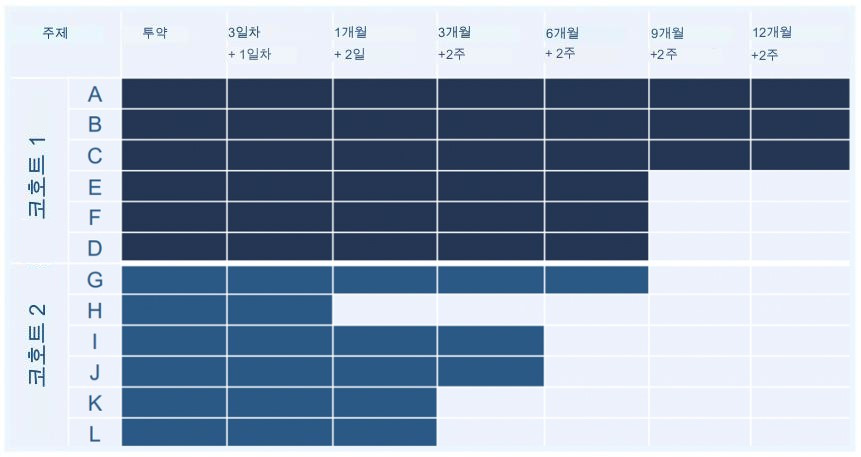
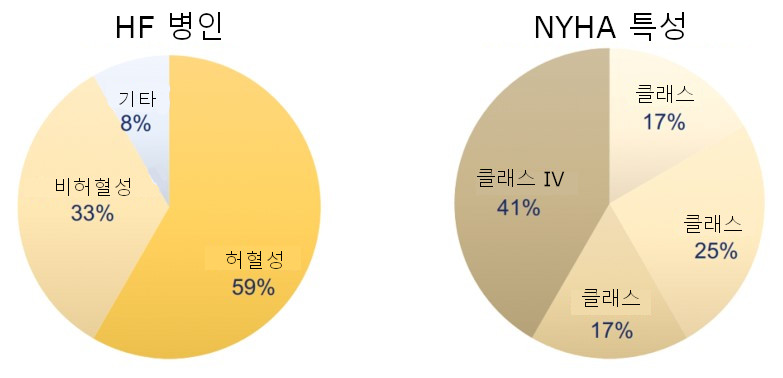
기준선에서 심부전 특성
6분 걷기 테스트 - LVAD에서 걸은 거리
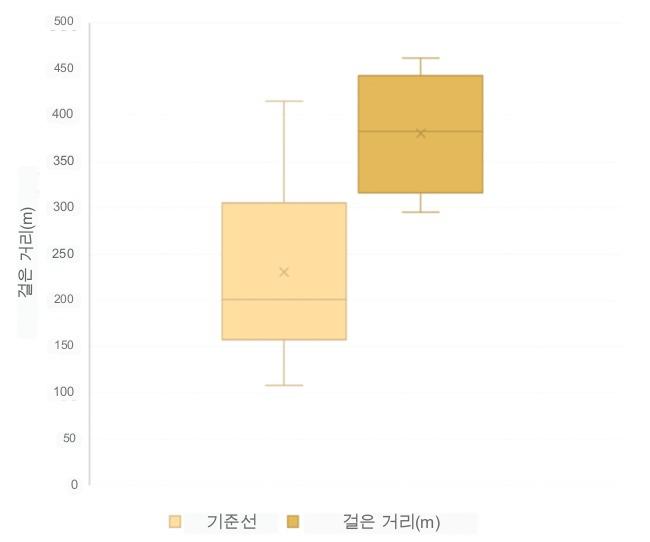
6분 도보 테스트 거리
GENEX-3 치료 6개월 후, 이동 거리가 증가함에 따라 6분 걷기 테스트에서 더 나은 성능을 보이는 경향을 보였습니다.
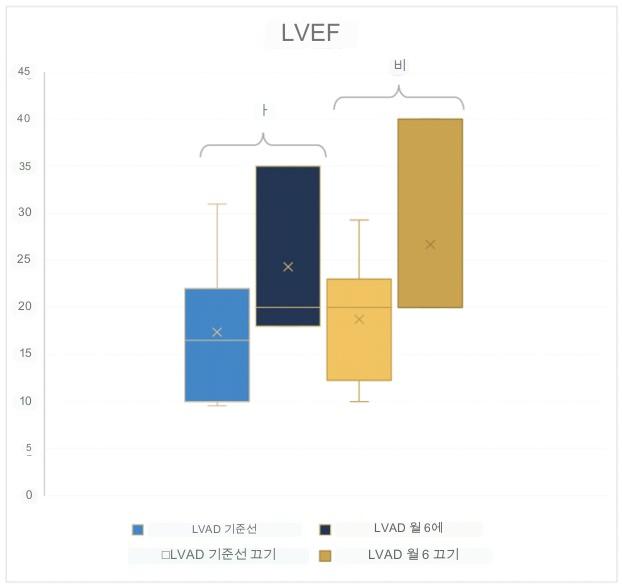
좌심실 박출률(LVEF)
GENEX-3 치료는 6개월 후 각 수축 동안 좌심실에서 펌핑되는 혈액의 양을 측정하는 좌심실 박출률(LVEF)에 긍정적인 영향을 미치는 것으로 나타났습니다.


